飞纳 Pharos-STEM 在细胞生物学和病理学的应用
一直以来,透射电镜(TEM)是观察和研究超微结构的首选工具,可用于观察整个细胞结构,包括细胞壁、细胞膜、细胞核和各种细胞器的变化,以及外源物质与细胞之间的关系等。不仅有助于许多重要细胞器的结构和功能的研究,而且有助于解剖病理学、血液学和微生物学等学科的病理诊断研究。
扫描透射(STEM)模式作为 TEM 的附加配件,可以显著提高生物样品的衬度,特别是未染色的组织切片。应对此类生物样品,TEM 操作人员通常也会选择相对较低的加速电压(80kV)来增加图像的衬度,并提高清晰度。但是由于其操作的复杂性,在对细胞生物学和病理学的超微结构的研究中,还没有被广泛应用(除专业的电镜中心外)。
飞纳台式场发射扫描电镜,体积小巧,具有低电压成像的优势,配备了新型的扫描透射(STEM)探测器后,可以结合扫描电镜和透射电镜的功能特点,在 15kV 的低加速电压下,就可以获得高分辨率的扫描透射成像。在观测电子束敏感的生物样品时,可以获得高成像质量图片。
以下为大家分享生物组织样品的制样方法以及 4 个使用 Pharos-STEM 拍摄的案例。(加速电压 15kV,工作距离 8.9mm)
具体过程如下:使用 2.5% 的戊二醇溶液(溶解于 PH 值为 7.4 的 0.1M 碳酸钠缓冲液中)进行固定,固定完成后,组织样品在碳酸钠缓冲液中清洗 1-2 天。这个过程具体包括使用 2% 四氧化饿清洗 4h,2% 醋酸铀清洗 1h,醋酸钠清洗 1h;然后使用梯度乙醇和丙酮进行脱水处理;接着按照标准配方使用低粘度环氧树脂 Spurr 进行包埋,将树脂在 70℃ 下固化 15h;最后使用超微切片机制备 70nm 厚的组织切片,将组织切片安装在 300 目的铜网上。接下来将具有样品的铜网放入 Pharos-STEM 中进行观测,结果如下。
案例一:被肾小囊(Bowman's capsule)包裹的正常肾小球
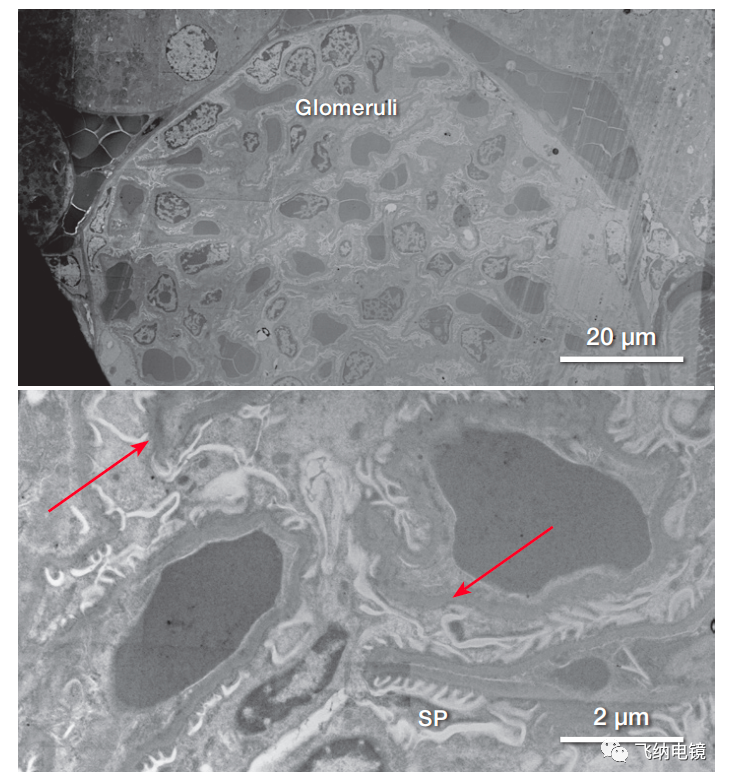
图1 小鼠肾标本样品(肾小球和临近的肾血管)的 STEM 图。红色箭头处可以看到含有红细胞的肾小球毛细血管,毛细血管被肾小球基底膜和足细胞的足突包围。
图1 为被肾小囊(Bowman's capsule)包裹的正常肾小球的超微结构。 STEM 图显示了正常肾小球毛细血管袢和肾小球系膜,与 TEM 下的微观图像类似。STEM 图中的红色箭头处清晰显示了肾小球基底膜、系膜基质、系膜胞质、足细胞足突的细节以及与基底膜毗邻的裂孔结构。STEM 图像显示了高分辨的超微结构,图像衬度明显,可以快速捕捉到极小的细胞变化,并快速分析感兴趣部位的微观结构。
案例二:正常的小鼠胰腺腺泡细胞

图 2 正常的小鼠胰腺腺泡细胞结构 STEM 图。图中显示了酶原颗粒(Z)、液泡、线粒体(M)、腺泡腔(L)和粗面内质网(R)。上图为胰腺星形细胞,下图为内质网的精细结构。
案例三:人类脑肿瘤组织
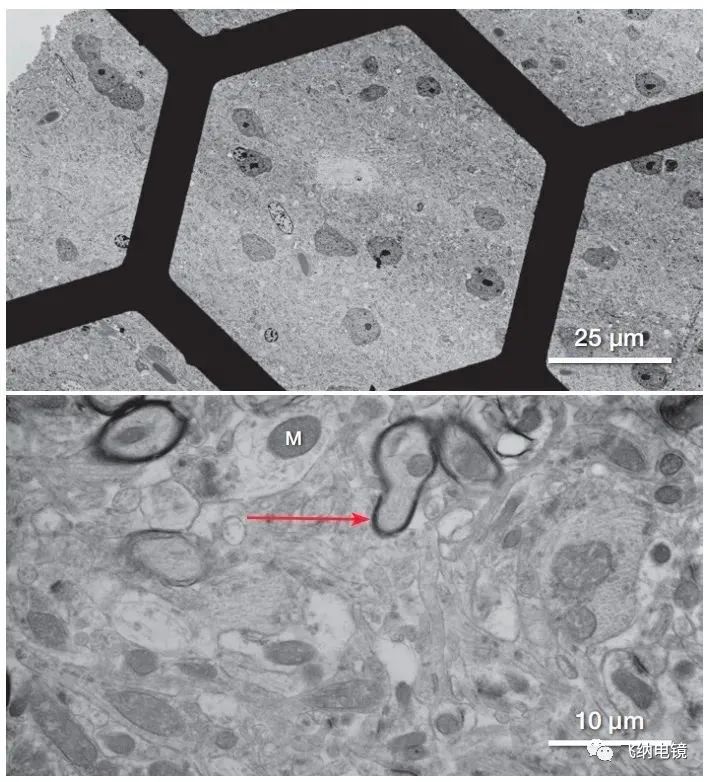
图 3 人类脑肿瘤组织 STEM 图。图中清晰显示了细胞的超微结构特征,髓鞘轴突、线粒体和嵴结构(M)、包含细胞间质纤维和囊泡的星形细胞结构(红色箭头处)。图中可以清晰观测到细胞结构和细胞器之间的关系。

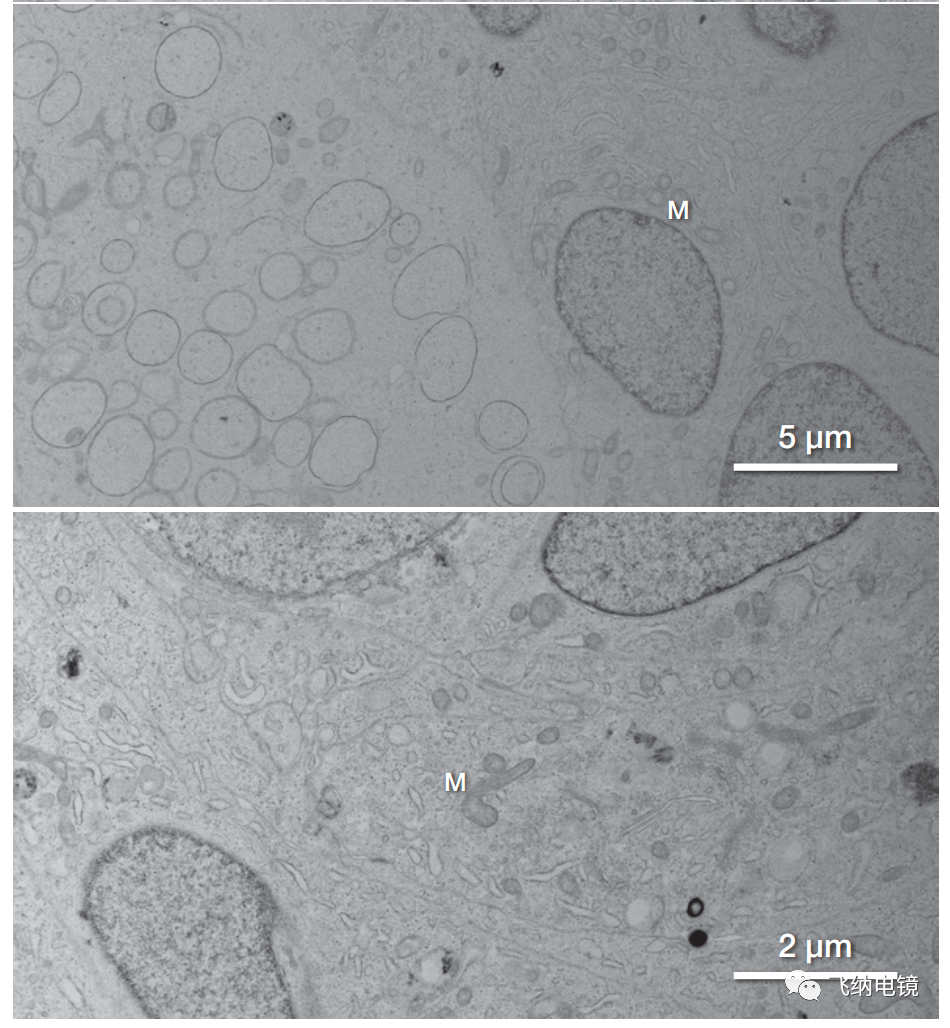
图4 培养的全能干细胞的 STEM 图。晶状体上皮细胞内有大量的细胞质器,如线粒体和卵圆形细胞核。均质的细胞外观与早期细胞分化阶段的细胞相似(数据来自 ROR1e LECs)。图中可以清晰看到晶状体的微结构,包括靠近组织周围的晶状体上皮细胞,以及与之相邻的具有杆状细胞核的未成熟的晶状体纤维细胞,具有圆形细胞核的细胞和晶状体纤维细胞类似。
总结
通过以上 4 个案例,可以看出,使用配备 STEM 探测器的飞纳台式场发射扫描电镜,在观察生物类样品时,在较低的加速电压下,几分钟内便可以获得高衬度、高分辨图像。如您对此产品感兴趣,欢迎联系我们。
参考文献
Cohen Hyams T; Mam K; Killingsworth MC, 2020, ‘Scanning electron microscopy as a new tool for diagnostic pathology and cell biology’, Micron, vol. 130, pp. 102797 -102797,
C. U., Devi, M. Masona, T. Cohen Hyams, M. C. Killingsworth, D. G. Harmana V. Gnanasambandapillai, L. Liyanage and M. D. O’Connor, ‘A simplified method for producing human lens epithelial cells and light-focusing micro-lenses from pluripotent stem cells’, Experimental Eye Research (2020)
 1942
1942
 0
0- 1工业三辊机工艺选型量化打分指南与全球品牌对照表
- 2半导体封装电子浆料(导电胶大功率散热膏)超细剪切工艺规范
- 3固态电池电解质及高镍正极浆料的高效脱泡与均匀搅拌技术指南
- 4JV选选粉机说明书
- 5SF人工砂石说明书
- 6超细粉
- 7TS-CX超细粉分级机说明书(1)
- 8三辊机高精度作业指南及安全自检手册

- 【助力科研】粉末挤出3D打印破解多材料梯度惰性阳极烧结开裂难题,推动无碳铝电解发展
- 粉末挤出3D打印制备难熔金属和先进陶瓷发展趋势
- 顶刊速递|为什么温敏水凝胶的研究进展值得关注?
- 声共振机械合金化 制备Ni-Al反应材料的可行性研究与机理探讨
- 突破肽类高浓度制剂瓶颈 声共振技术实现稳定纳米悬浮
- 常驻顶刊!为何磁性纳米粒子的研究如此“高产”?
- 日本石川擂溃机化学工业实验用装置的高效选择
- 为什么COFs的催化应用近期顶刊不断?
- 从“作用”到“场域”:粉碎技术的范式演进与柯立微能量场理论的构建
- 大明化学氧化铝粉在低温烧结制粉中的应用
- Development, Characterization, and Molecular Dynamics Simulation of Andrographolide Nanosuspensions Utilizing Hummer Acoustic Resonance Technology
- 苏州碳丰科技首席科学家程金生老师以本公司名义在国际上发表关于石墨烯纤维的论文《石墨烯纤维纳米复合材料的合成及氨基酸检测的分析应用》:
- 介可视·散装物料库存管理雷达全景扫描系统在料仓、堆场中的应用
- 磷酸化修饰鬼臼果多糖的制备及生物活性
- DSR论文解读:Advanced Science News 报道中科院长春应化所新型非铂催化材料研究成果
- High-throughput preparation, scale up and solidification of andrographolide nanosuspension using hummer acoustic resonance technology(纳米混悬剂制备的前瞻性技术 - 蜂鸟声共振)

